Op 25 en 26 september 2014 organiseerden de European Atherosclerosis Society (EAS) en de European Federation of Clinical Chemistry and Laboratory Medicine (EFLM) hun eerste gemeenschappelijke symposium in het concertgebouw van Brugge, de “Atherosclerosis and Cardio-Endocrine Biomarkers Course”. Prof. dr. Michel Langlois trad op als voorzitter namens de Belgian Lipid Club en de dienst Laboratoriumgeneeskunde van het AZ Sint-Jan Brugge-Oostende AV. Internationale opinieleiders gaven er – voor een multidisciplinair publiek van endocrinologen, cardiologen, huisartsen, klinisch biologen en laboratoriumtechnologen – hun visie over nieuwe biomerkers voor het management van dyslipidemie en de preventie van atherosclerose en cardiovasculaire ziekte. Hierna volgt een verslag van enkele relevante presentaties voor de klinische praktijk.
De LDL-hypothese houdt stand
Volgens de experten blijft de verlaging van LDL-cholesterol de primaire, evidentiegebaseerde doelstelling voor de preventie van cardiovasculaire ziekte gerelateerd aan hyperlipidemie. De LDL-streefwaarde van < 100 mg/dl wordt aanbevolen bij elke patiënt met een hoog cardiovasculair mortaliteitsrisico, te berekenen met het Europese SCORE-model.[1] Interventiestudies met hypolipemiërende medicatie (statines) tonen consistent aan dat elke LDL-daling van 40 mg/dl resulteert in een vermindering van coronaire hartaandoeningen van maar liefst 20% in de populaties, wat wijst op de belangrijke gezondheidseconomische impact van een goede preventiestrategie.
De bekendgemaakte resultaten van de IMPROVE-IT studie met ezetimibe bevestigen mooi deze LDL-hypothese. Ezetimibe vermindert de intestinale absorptie van cholesterol. De studie beantwoordt een aantal tot nu toe onopgeloste vragen, namelijk dat een substantiële LDL-verlaging – zelfs onder de 70 mg/dl – het cardiovasculaire risico nog significant meer verkleint (”even lower is even better”) en dat het toevoegen van ezetimibe bij een statine effectiever is dan statinemonotherapie. Mogelijke indicaties voor ezetimibetherapie zijn een persisterend hoge LDL-cholesterol onder statinebehandeling of ezetimibemonotherapie bij statine-intolerantie.
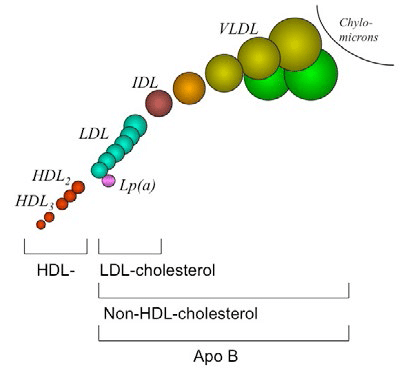
Lipoproteïnen van verschillende grootte en densiteit gescheiden na ultracentrifugatie van plasma en hun representatieve laboratoriummerkers bij nuchtere bloedafname. (HDL: hoge densiteit lipoproteïnen, LDL: lage densiteit lipoproteïnen, IDL: intermediaire densiteit lipoproteïnen, VLDL: zeer lage densiteit lipoproteïnen, Lp(a): lipoproteïne(a), apoB: apolipoproteïne B)
Nieuwe therapeutische doelstellingen: non-HDL-cholesterol en apoB
Alle klinische studies met statines tonen een niet te verwaarlozen residueel risico voor cardiovasculaire aandoeningen bij 70 à 80% van de behandelde patiënten, ondanks het behalen van de LDL-streefwaarden. Dit kan deels worden toegeschreven aan het blijven voortbestaan van dyslipidemieën zoals een laag HDL-cholesterol, hoge triglyceriden of een gecombineerde hyperlipidemie, en in die omstandigheden is de hoeveelheid LDL-cholesterol onvoldoende representatief voor het atherosclerosegerelateerde risico.
Naast de “slechte” LDL-partikels bevinden zich nog andere atherogene lipoproteïnen in de bloedcirculatie, met name VLDL, IDL en Lp(a). De totaliteit van al deze “schadelijke” cholesterolfracties wordt gereflecteerd door de non-HDL-cholesterol (zie figuur 1). Deze test berekent het verschil tussen de gemeten totale cholesterol en de “goede” HDL-cholesterolwaarden en is dus kosteloos.
Wanneer non-HDL-cholesterol bepalen?
- Bij patiënten met een persisterende dyslipidemie onder statinebehandeling is de non-HDL-cholesterol sterker gecorreleerd met de cardiovasculaire prognose dan de LDL-cholesterol. Bijgevolg is de non-HDL-cholesterol te gebruiken als secundaire therapeutische doelstelling na het behalen van de LDL-streefwaarden bij die patiënten waarbij de VLDL-partikels belangrijker zijn: hypertriglyceridemie, diabetes, metabool syndroom, chronische nierinsufficiëntie (zie tabel 1). Het verlagen van de non-HDL-cholesterol zal het residuele hartrisico effectief verkleinen.[2] Dit moet in de eerste plaats gebeuren door het voorschrijven van een krachtiger statine of een hogere dosering (indien deze goed wordt verdragen). Indien dit onvoldoende is, kan naast de statine nog een fibraat (voor het verlagen van de triglyceriden) of ezetimibe voorgeschreven worden.
- Wanneer de LDL-cholesterol niet beschikbaar is. Bij hypertriglyceridemie > 400 mg/dl is een accurate LDL-bepaling in de laboratoria niet mogelijk.
Om deze redenen wordt de non-HDL-cholesterolberekening steeds aanvullend gerapporteerd door het laboratorium zonder meerkost voor de patiënt. De EAS-richtlijnen suggereren apolipoproteïne B (apoB) als alternatief secundair doelwit van cardiopreventieve therapie (zie tabel 1). ApoB is het apoproteïne aanwezig op alle atherogene LDL- en VLDL-partikels. De apoB-bepaling in het laboratorium is technisch veel accurater maar wel duurder dan de (kosteloze) berekening van de non-HDL-cholesterol.
|
Tabel 1: Primaire en secundaire therapeutische streefwaarden volgens SCORE |
|||
| Risico (SCORE**) | LDL-cholesterol (mg/dl) | Non-HDL-cholesterol* (mg/dl) | ApoB* (g/l) |
| ≥ 10% *** | <70 | <100 | <0.8 |
| 5 – < 10% | <100 | <130 | <1.0 |
| * Secundair therapeutisch doelwit bij patiënten met gecombineerde dyslipidemie, metabool syndroom, type 2 diabetes of chronisch nierlijden. ** SCORE: Systematische COronaire Risico Evaluatie (% 10-jaarsrisico op fatale cardiovasculaire ziekte). *** Zeer hoog mortaliteitsrisico incl. patiënten met cardiovasculaire ziekte, gecompliceerde diabetes of nierinsufficiëntie. |
|||
Familiale hypercholesterolemie wordt ondergediagnosticeerd
Familiale hypercholesterolemie (FH) kenmerkt zich door zeer hoge LDL-cholesterolwaarden op basis van een autosomaal dominante genetische oorzaak, meestal een mutatie in het gen voor de LDL-receptor en soms ook in het apoB (het apoproteïne noodzakelijk voor binding aan de LDL-receptor) of het PCSK9 (inhibitor van de LDL-receptor). Door een verminderde opname van LDL-partikels in de cellen via de LDL-receptoren stijgt de LDL-cholesterolhoeveelheid in het bloed. De geschatte prevalentie van heterozygote FH is 1/200 maar vele gevallen worden niet gediagnosticeerd. Homozygote FH is zeldzaam (1/106). Vermits deze personen reeds vanaf een jonge leeftijd blootgesteld zijn aan hoge aantallen LDL-partikels lopen ze een zeer hoog risico op het vroegtijdig ontwikkelen van atherosclerose en coronair hartlijden.[3]
De meest efficiënte manier om FH op te sporen is, vertrekkende van een individuele casus, proactief de familie in cascade te screenen en een ‘LDL-stamboom’ op te stellen om zo niet gekende gevallen vroegtijdig op te sporen. Men gebruikt de DLCN-score (Dutch Lipid Clinic Network) en genetisch onderzoek wordt aanbevolen indien de DLCN-score meer dan 5 bedraagt (zie tabel 2).
Wanneer denken aan familiale hypercholesterolemie?
FH moet worden opgespoord bij volwassenen met een totaal cholesterolgehalte van > 310 mg/dl, kinderen met een totaal cholesterolgehalte van > 230 mg/dl, of in het geval van vroegtijdig coronair hartlijden, peesxanthomen of een gekend familielid met FH en/of vroegtijdig cardiaal lijden.
Bij het familiaal voorkomen van vroegtijdig atherotrombotisch lijden dient ook de Lp(a) bepaald te worden.[3] Deze onafhankelijke genetische risicofactor vertoont een sterk synergistisch effect met LDL-cholesterol. Bij een hoge Lp(a) verdubbelt het cardiovasculaire risico, maar Lp(a) in combinatie met een hoge LDL-cholesterol verviervoudigt het risico!
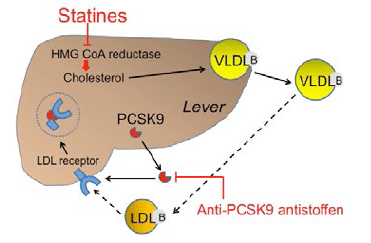
Figuur 2: De LDL-cholesterolcyclus van de lever en therapeutische aangrijpingspunten: Het enzym HMG-CoA-reductase staat in voor de synthese van cholesterol, dat samen met apoB en triglyceriden wordt opgenomen in de VLDL-partikels geproduceerd door de lever. In de bloedcirculatie worden VLDL-partikels omgezet naar LDL-partikels, die in de cellen worden opgenomen door LDL-receptoren via binding aan apoB. Na endocytose wordt cholesterol vrijgemaakt uit het vesikel en de LDL-receptor wordt intact gerecycleerd naar de celmembraan. Statines werken cholesterolverlagend door de inhibitie van HMG-CoAreductase en stimuleren onrechtstreeks (via intracellulaire cholesteroldaling) de expressie van LDL-receptoren maar ook van PCSK9. Het eiwit PCSK9 blokkeert de recyclage van de LDL-receptoren na endocytose. De toevoeging van PCSK9- antistoffen aan statinetherapie inhibeert de PCSK9-blokkade van LDL-receptoren, waardoor veel meer LDL-cholesterol verwijderd kan worden uit de bloedcirculatie.(HMG-CoAreductase: 3-hydroxy-3-methylglutaryl-co-enzym-A-reductase, PCSK9: proproteïne convertase subtilisin/kexin type 9)
Nieuwe therapeutische ontwikkelingen
Ondanks de enorme sprong voorwaarts dankzij de introductie van statines is verder innovatief onderzoek nodig om de dyslipidemieën nog beter onder controle te brengen met als doel cardiovasculaire ziekte te voorkomen. Tegenwoordig zijn nieuwe producten in ontwikkeling, zoals PCSK9-inhibitoren en apoBsynthese-inhibitoren. Vooral de PCSK9-inhibitoren lijken beloftevol. PCSK9 is een eiwit dat de LDL-receptor blokkeert en aldus het LDL verhoogt (zie figuur 2). De anti-PCSK9- inhibitoren in ontwikkeling zijn monoclonale antistoffen die de werking van het eiwit blokkeren, waardoor veel meer LDL-cholesterol verwijderd kan worden uit het bloed. Momenteel worden deze producten getest op effectiviteit en veiligheid bij de mens. Studies tonen een spectaculaire verlaging (tot 60%) van de LDL-cholesterol en openen perspectieven voor de behandeling van FH, waar statines meestal ontoereikend zijn.[4]
Besluit
Klassieke lipidentesten en een aantal evidentiegebaseerde nieuwe merkers zijn klinisch performant maar hebben ook hun beperkingen. De dienst Laboratoriumgeneeskunde van het AZ Sint-Jan Brugge-Oostende AV blijft daarom actief in het wetenschappelijk onderzoek en de validatie van nieuwe biomerkers voor het vroegtijdig opsporen van atherosclerose. Met de organisatie van de Europese EAS-EFLM-conferentie te Brugge bevestigt het laboratorium zijn voortrekkersrol in het cardiovasculaire preventiebeleid op nationaal en internationaal gebied.
|
Tabel 2: Diagnostische criteria voor heterozygote familiale hypercholesterolemie volgens DLCN-score |
|||
| Criteria | Score | ||
| Familiale voorgeschiedenis | Eerstegraadsfamilielid met vroegtijdig coronair hartlijden* en/of LDL > 200 mg/dl | 1 | |
| Eerstegraadsfamilielid met peesxanthomen en/of kinderen < 18 jaar met LDL > 135 mg/dl | 2 | ||
| Klinische voorgeschiedenis | Patiënt heeft vroegtijdig coronair hartlijden* | 2 | |
| Patiënt heeft vroegtijdig cerebrale/perifere vasculaire ziekte | 1 | ||
| Lichamelijk onderzoek | Peesxanthomen | 6 | |
| Arcus cornealis voor de leeftijd van 45 jaar | 4 | ||
| LDL-cholesterol | > 330 mg/dl | 8 | |
| > 250-329 mg/dl | 5 | ||
| > 190-249 mg/dl | 3 | ||
| > 155-189 mg/dl | 1 | ||
| Zeker FH | score > 8 | ||
| Waarschijnlijk FH | score 6-8 | ||
| Mogelijk FH | score 3-5 | ||
| Geen diagnose | score < 3 | ||
| *Mannen vóór hun 55ste levensjaar, vrouwen vóór hun 60ste levensjaar. | |||
Download het artikel als PDF-bestand.
Copyright © 2015 AZ Sint-Jan Brugge-Oostende AV. Alle rechten voorbehouden. De inhoud (zowel teksten als afbeeldingen) van dit magazine is auteursrechtelijk beschermd. Niets uit deze uitgave mag vermenigvuldigd of doorgegeven worden aan derden zonder schriftelijke toelating van de uitgever.