Chronische pijn komt steeds vaker voor in onze samenleving. Een effectieve behandelingsmethode is dan ook noodzakelijk. Voor chronische pijnpatiënten bij wie alle andere therapieën gefaald hebben, kan Ziconotide een oplossing bieden.
De farmacologie van Ziconotide
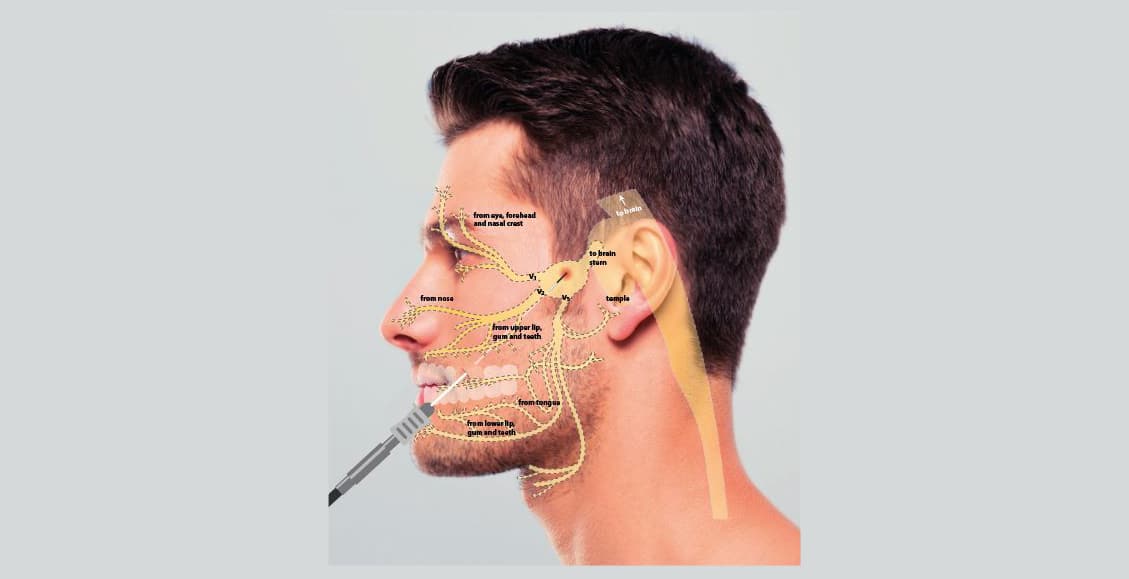
Ziconotide is het synthetische analoog van ω-conopeptide, afkomstig uit het gif van de piscivorous slak (conus magus). Het 25-aminozuurpeptide bindt selectief en met hoge affiniteit aan de η-Type calcium kanalen, die in grote hoeveelheid gelokaliseerd zijn in de dorsale hoorn van het ruggenmerg. Op deze plaats maken de primaire pijnafferenten hun eerste synaps met de tractus spino-thalamicus, die de pijnsignalen doorstuurt naar de hersenen. Ziconotide blokkeert de calcium influx en inhibeert daardoor de neuronenexitabiliteit en neurotransmissie. De binding is volledig maar reversibel. Ziconotide bindt niet op de opiaatreceptoren en heeft daarom een verschillend farmacologisch profiel. Het geeft geen aanleiding tot ademhalingsdepressie, tolerantie of fysieke afhankelijkheid. De behandeling kan op elk moment zonder ernstige abstinentiesymptomen onder broken worden. Ziconotide passeert de bloed- en hersenbarrière niet. Daarom moet het intrathecaal (IT) worden toegediend.
Ziconotide wordt binnen het CSV (cerebrospinaal vocht) hoofdzakelijk verdeeld door bulkstroom. De halfwaardetijd (T½) in CSV bedraagt vierenhalf uur. De penetratie in het ruggenmerg gebeurt zeer traag en kan tot enkele dagen in beslag nemen. Ziconotide wordt niet gemetaboliseerd in het liquor. Na passage in de systeemcirculatie wordt het door diverse peptidasen en proteasen gemetaboliseerd. Dosisreductie bij lever- of nierfalen is dus niet noodzakelijk. De gemiddelde T½ in plasma is 1,3 uur. Door de trage weefselpenetratie wordt geadviseerd om de dosering te starten aan 2,4 µg per dag en op individuele basis te titreren, afhankelijk van het pijnstillend effect en de nevenwerkingen. Een trage en geleidelijke opdosering van 2,4 µg per dag tot een maximumdosis van 21,6 µg per dag is noodzakelijk. Het geadviseerde interval tussen dosisverhogingen is 48 uur of meer.
Chronische pijn
Chronische pijn is een vaak voorkomend probleem in onze maatschappij. Een succesvolle behandeling ervan vereist meer dan enkel pijnreductie. Chronische pijnpatiënten geraken vaak sociaal en economisch geïsoleerd, wat tot depressie en emotionele uitbarstingen kan leiden. Een negatieve mentale ingesteldheid verergert vaak de pijn. Daarom is een multidisciplinaire benadering van deze patiënten noodzakelijk.
Wanneer alle conservatieve behandelingen falen, komt de patiënt in aanmerking voor meer geavanceerde neuromodulaire technieken, zoals ruggenmergstimulatie (SCS) of intrathecale analgetica-toediening (ITA). Wij verkiezen SCS boven gecombineerde orale opiaten en ITA, hoewel bepaalde chronische pijnen beter aan ITA dan aan SCS beantwoorden.
Medicatie proefperiode
Sinds 1997 wordt in België de implantatie van elektronische pompsystemen geregeld door de ziekteverzekering. Enkel langdurige neurogene pijnsyndromen, afkomstig uit het centraal zenuwstelsel, het ruggenmerg en de perifere zenuwen of na trauma van een perifere zenuw, komen in aanmerking voor implantatie van neuromodulaire systemen, en dit slechts wanneer er aan bepaalde selectiecriteria wordt voldaan – het falen van verschillende conservatieve therapieën, geen indicatie voor chirurgie, geen ernstige medicatie-abusus en geen contra-indicatie voor implantatie ( bijvoorbeeld infectie- of bloedstoornis). Bovendien moeten de patiënten een psychiatrische en psychologische evaluatie ondergaan en meer dan de helft pijnvermindering tijdens een proefperiode van vier weken bereiken. Na evaluatie van de patiënten moet er een verbetering van levenskwaliteit, normale dagelijkse activiteit en pijnscore en een verminderd gebruik van bijkomende pijnmedicatie aangetoond kunnen worden.
Deze proefperiode is niet alleen belangrijk voor de persoonlijke besluitvorming van de patiënt en de evaluatie van bijwerkingen, maar ook voor de individuele dosering van de verschillende uitgeteste analgetica. De proef moet altijd via IT weg uitgevoerd worden. Als er sterk hydrofiele medicatie wordt toegediend in de intrathecale of epidurale ruimte, kan het klinisch effect sterk variëren.
Wij verkiezen IT katheters te gebruiken die via een port-a-cath systeem met een externe pomp worden verbonden. Er is weinig gevaar voor complicaties en een verlaagd risico voor meningitis wanneer een strikt aseptische techniek wordt toegepast en wanneer de vulling die door de proef wordt gebruikt onder laminaire airflow wordt bereid.
Wij gaan enkel over tot pompimplantatie wanneer de patiënt aan de volgende criteria voldoet: strikte indicatie, multidisciplinaire evaluatie, consensus en een succesvolle proefperiode.
Langetermijn- en neveneffecten
De doeltreffendheid van opiaten op lange termijn hangt af van het soort pijn, de verandering in pijnintensiteit, de ontwikkeling van tolerantie (met inbegrip van mogelijke cross-tolerantie tussen verschillende opiaten) en genetische verschillen in tolerantie. Veranderingen in psychologische status of technische problemen met het leveringssysteem kunnen ook zorgen voor een verminderde doeltreffendheid. Dezelfde factoren zijn op Ziconotide van toepassing, behalve dat er geen evidentie is van tolerantie. Enkel titratie en liquor bulkstroom kunnen de doeltreffendheid van Ziconotide beïnvloeden. Een andere nevenwerking van opiaten is de ontwikkeling van fysieke afhankelijkheid, wat serieuze ontwenningsverschijnselen in geval van problemen met de toediening kan veroorzaken. Addictie, veeleer een psychologisch dan een fysiek probleem, wordt gewoonlijk niet gezien bij toediening van IT opiaten omdat het een artsgecontroleerd systeem betreft. De patiënt kan de dosis zelf niet wijzigen. Er is geen evidentie voor fysieke afhankelijkheid of addictie bij het gebruik van Ziconotide.
De meest voorkomende nevenwerkingen van opiaten zijn farmacologisch (nausea, jeuk, urineretentie, constipatie) en hormonaal (seksuele dysfunctie, vochtretentie). Het is ook mogelijk dat er zich granuloma vormen aan het uiteinde van de catheter. Deze bijwerkingen verdwijnen gewoonlijk na stopzetting van de toediening van opiaten. Dosisvermindering van een opiaat heeft nochtans geen invloed op het optreden van deze bijwerkingen. Nevenwerkingen van Ziconotide zijn meestal neurologisch en adequaat behandelbaar door een kleine dosisaanpassing of het volledig stopzetten van de toediening. Er is geen evidentie van hormonale dysfunctie of vorming van granuloma met Ziconotide.
Conclusie
Ziconotide is een welgekomen aanvulling bij de huidige behandelingsopties voor patiënten met ernstige chronische refractaire pijn bij wie alle conservatieve therapieën hebben gefaald. Belangrijk is de vereiste langzame titratie van Ziconotide om nevenwerkingen te vermijden. Ziconotide heeft ook een geïndividualiseerd therapeutisch luik. Daarom mag het enkel worden toegediend door specialisten die een ruime ervaring hebben in IT therapie.
Case Report 1
In deze case wordt een langdurige ervaring beschreven met IT Ziconotide bij een 55-jarige mannelijke patiënt met chronische pijn als gevolg van diverse lage rugoperaties. Alle conservatieve, chirurgische behandelingen en de toediening van IT morfine hebben gefaald. De patiënt kwam in aanmerking voor een placebo-gecontroleerde studie waarbij Ziconotide getest werd op doeltreffendheid en veiligheid. Na een succesvolle behandeling op korte termijn werd hij opgenomen in een vervolgstudie op lange termijn. Het dosisregime, het begin en de resolutie van neveneffecten (AEs) en de verbetering op de Visuele Analoge Schaal van Pijn Intensiteit (VASPI) werden bekeken. De patiënt reageerde in het algemeen positief op Ziconotide, hoewel er ernstige nevenwerkingen optraden als gevolg van een te snelle titratie.
Case Report 2
Deze case beschrijft het gebruik van Ziconotide bij een 39-jarige oude dame die een plexus avulsieletsel heeft opgelopen met als gevolg zuivere neuropathische pijn en neurologische schade in het L5 en S1 dermatoom van het rechtse been. Ze had ondraaglijke hormonale bijwerkingen van de IT morfine. De dosering van Ziconotide gebeurde zeer langzaam met een interval van twee of drie dagen tijdens de eerste twee weken en om de twee weken daarna. De startdosis was 0,1 µg per uur, verhoogd met 0,05 µg per uur bij ieder bezoek. Na zes maanden werd de toediening van parenterale morfine volledig stopgezet en de VASPI reduceerde tot 0 mm. Er waren enkel milde bijwerkingen, die met lichte dosisaanpassingen werden behandeld.