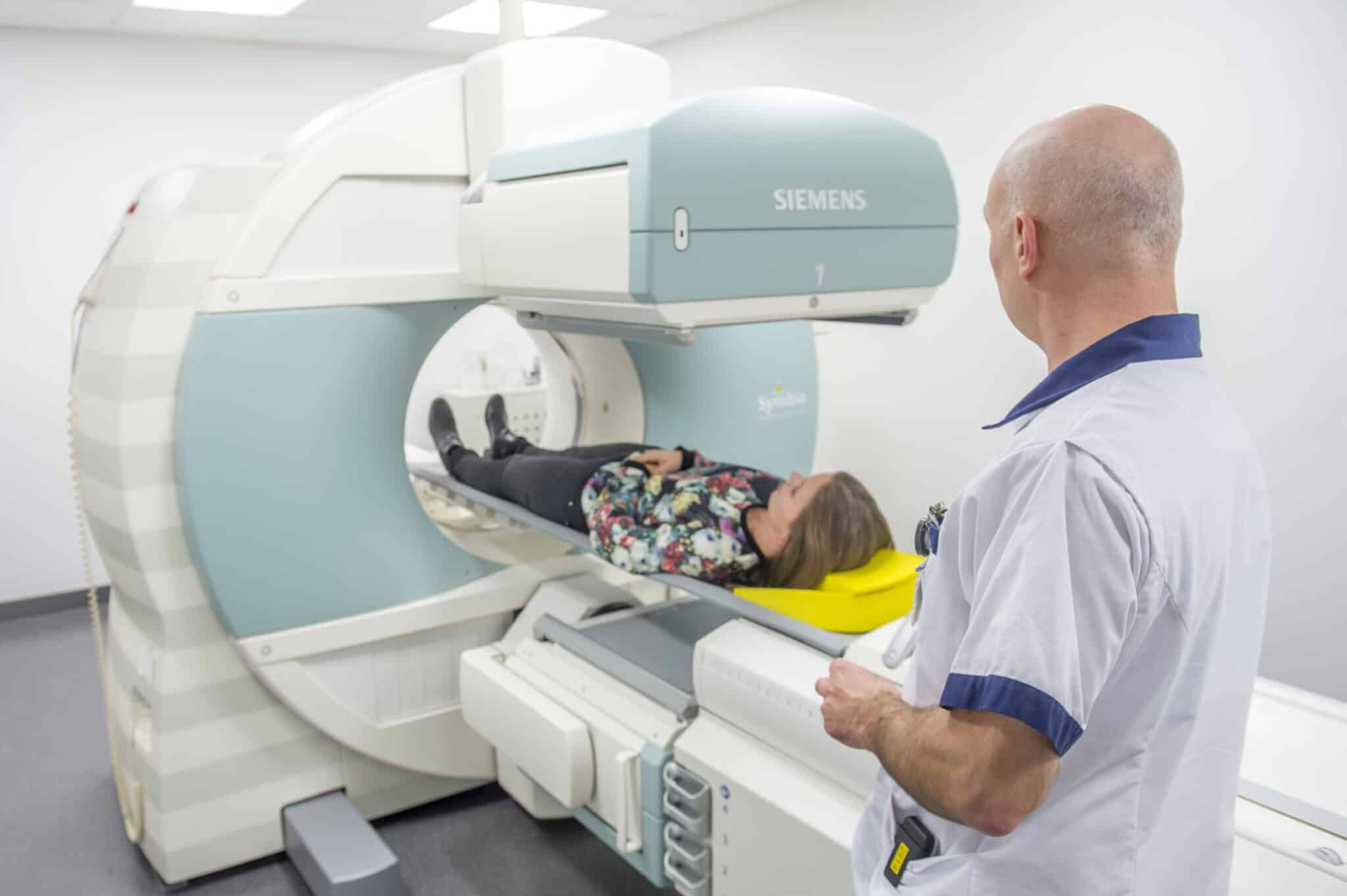
In de interventionele oncologie verscheen de voorbije jaren een “new kid on the block”, namelijk transarteriële radio-embolisatie (TARE), ook selectieve interne radiotherapie (SIRT) genoemd. De TARE-behandeling bestaat uit een katheterisatie van de patiënt via de lies om radioactief geladen micropartikels rechtstreeks in de arteria hepatica te injecteren. De bedoeling is om lokaal een zo hoog mogelijke dosis straling af te leveren in tumorale leverletsels.
Radioactief geladen micropartikels
TARE steunt op het fysiologisch principe dat gezonde hepatocyten preferentieel bloed krijgen vanuit de vena portae, terwijl het hoofdzakelijk de arteria hepatica is die levertumoren bevloeit. Radioactief geladen microsferen geïnjecteerd in de arteriële tak die voor de tumorale bloedvoorziening zorgt, komen definitief vast te zitten in de capillairen. De hypervascularisatie van de tumoren zorgt ervoor dat er relatief meer sferen terechtkomen in de letsels dan in het omliggende, niet tumoraal aangetaste leverweefsel.
Er zijn twee types micropartikels op de markt: glassferen (TheraSphere®) en harssferen (SIRSpheres®). Hoewel er een aantal verschillen zijn in de fysische eigenschappen en toedieningswijze, is hun efficiëntie vergelijkbaar. Het AZ Sint-Jan Brugge-Oostende AV maakt gebruik van harssferen. De lading van beide types sferen is Yttrium-90 (90Y), een radioactief element dat bij zijn verval pure β-straling afgeeft met een maximaal bereik van 1,1 cm. Dit betekent dat de straling hoofdzakelijk geconcentreerd blijft rond de depositieplaats van de sferen.
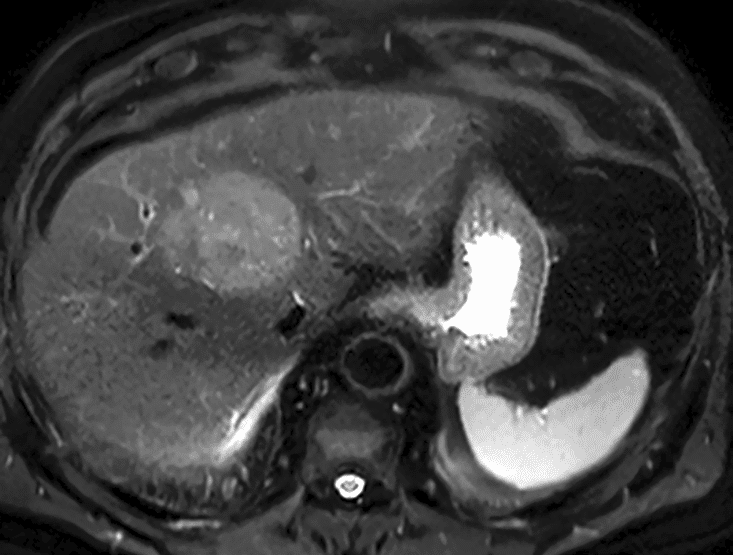
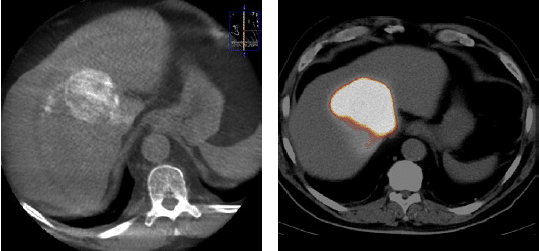
Deze MRI toont een solitair hepatocellulair carcinoom in een cirrotische lever op basis van hemochromatose. TARE wordt gepland om de tumorgroei onder controle te houden in afwachting van een levertransplantatie.
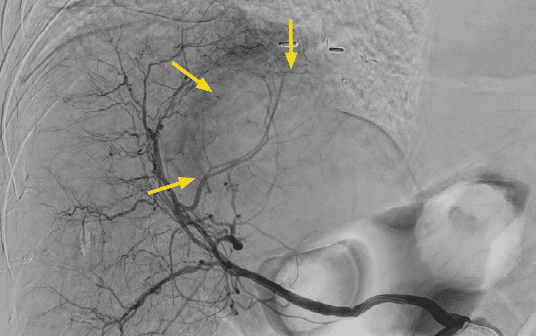
Dit angiografiebeeld werd genomen na het toedienen van een contrastmiddel in de rechter arteria hepatica. In tegenstelling tot de verwachtingen wordt de tumor niet bevloeid door dit bloedvat: er is een uitsparing te zien in de vascularisatie op de plaats waar de tumor zich bevindt (gele pijlen).
Behandelingsprocedure
De TARE-procedure verloopt in 2 fasen: na een diagnostische “work-up” volgt enkele weken later de eigenlijke behandeling. Bij de work-up voert de interventioneel radioloog een angiografie uit om het vascularisatiepatroon van de lever en tumor(en) zo gedetailleerd mogelijk in kaart te brengen (zie figuren 1 t.e.m. 4). Doel is om de optimale injectieplaats(en) van de sferen te bepalen. Het te behandelen doelvolume kan een solitair letsel zijn, een leversegment, een lob of de volledige lever.
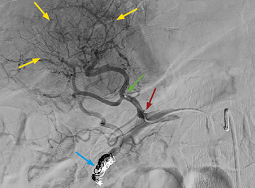
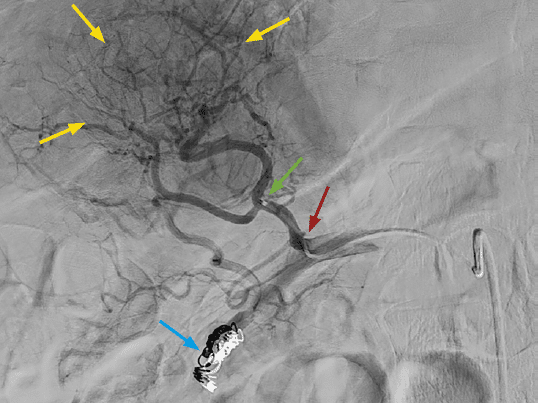
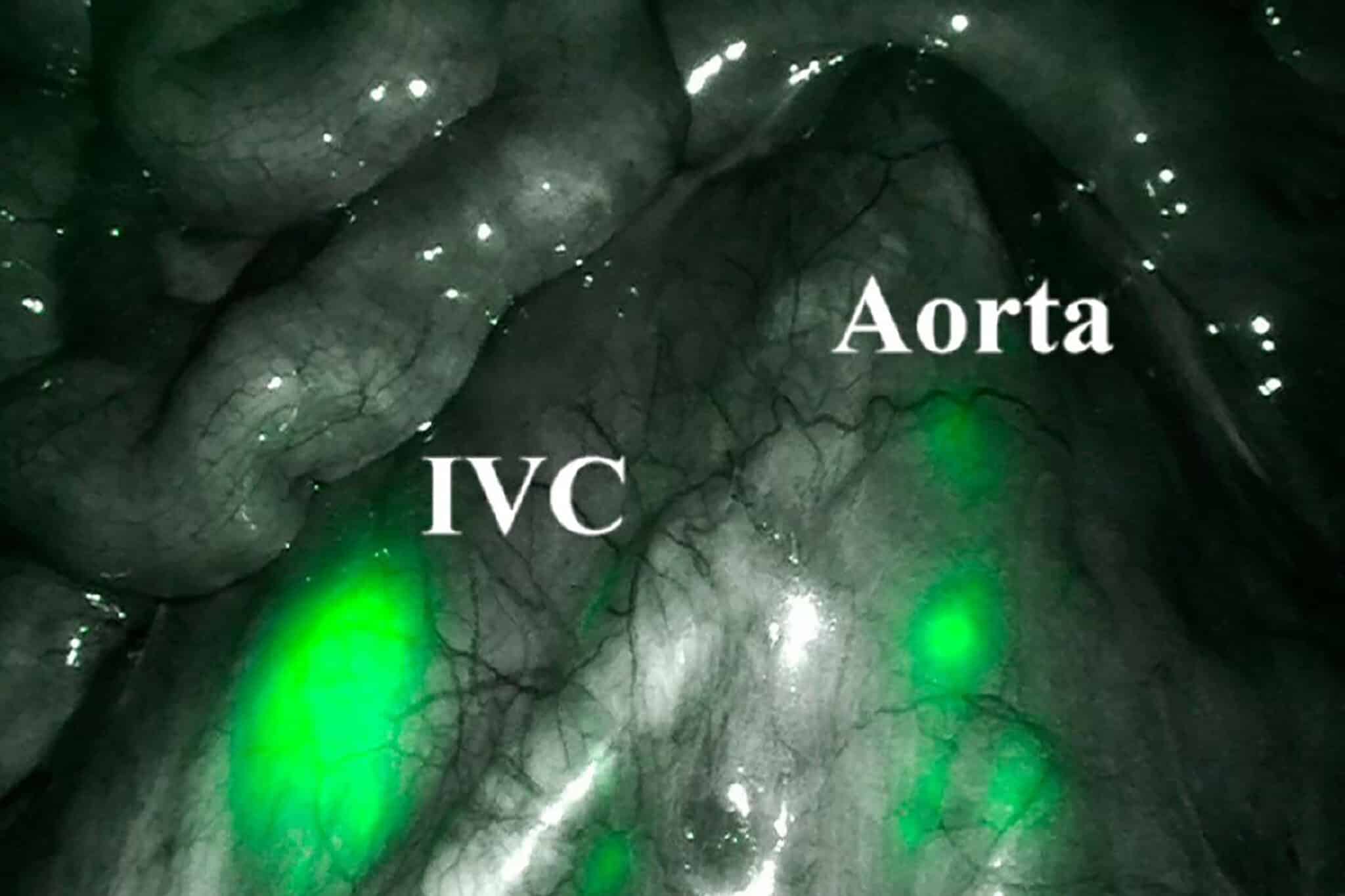
Fig.3 De tumor (gele pijlen) wordt bevloeid door een arterie die proximaal op de arteria gastroduodenalis ontspringt (rode pijl). Ter bescherming van de maag wordt het distale gedeelte van de arteria gastroduodenalis gecoiled (blauwe pijl). Contrast en 99mTc-MAA worden net voor de bifurcatie van het tumorvoedend bloedvat geïnjecteerd (groene pijl).
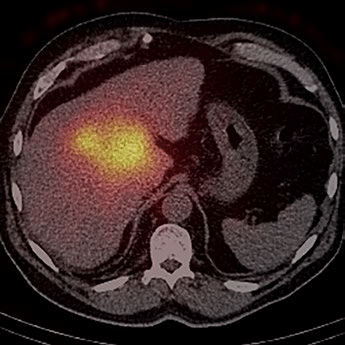
Fig.4-5 De cone beam CT-scan na contrastinjectie (links) en SPECT na 99mTc-MAA injectie (rechts) in het tumorvoedend bloedvat tonen de perfusie van de tumor en geen extrahepatische aankleuring.
Het is extreem belangrijk om te voorkomen dat sferen door reflux zouden terechtkomen in bloedvaten die andere abdominale organen bevloeien, zoals de maag, pancreas of galblaas, aangezien ze daar radionecrose kunnen veroorzaken. Afhankelijk van de specifieke vasculaire anatomie van de patiënt maakt de radioloog sommige arteriën daarom preventief dicht met metalen coils (zie figuur 3).
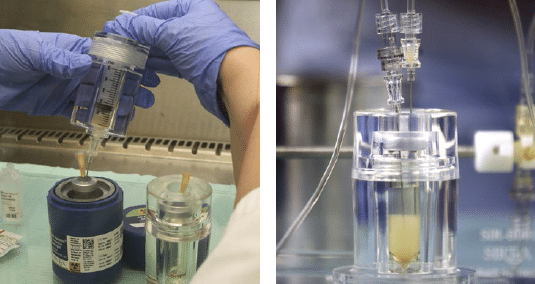
Fig.6 De dosis 90Y-geladen sferen wordt klaargemaakt in het hotlab op de dienst Nucleaire Geneeskunde, waarna ze in een plexi toedieningsbox geplaatst worden.
Wanneer de te volgen therapeutische strategie duidelijk is, wordt een dosis laagradioactieve simulatievloeistof (microaggregaten van albumine, gemerkt met Technetium-99m) ingespoten op exact dezelfde plaats waar men enkele weken later de eigenlijke 90Y-geladen sferen zal injecteren. De dienst Nucleaire Geneeskunde maakt vervolgens beelden om te controleren of het testproduct inderdaad in de geviseerde tumor(en) is terechtgekomen en of er geen onvoorziene extrahepatische tracerdepositie optrad (zie figuur 5).
Op de dag van de therapie wordt de vooraf berekende dosis 90Y-harssferen geprepareerd in het hotlab op de dienst Nucleaire Geneeskunde en in een speciale plexi box geplaatst. Deze wordt in de angiozaal geconnecteerd aan de toedieningskatheter (zie figuur 6). Zo kunnen de sferen langzaam intra-arterieel geïnstilleerd worden, waarna controle SPECT-beelden worden gemaakt (zie figuur 7).
Toepassing en bijwerkingen
Fig.7 De controle remstraling SPECT na toediening van de therapie wijst op een mooie focale depositie van de 90Y-geladen harspartikels in de tumor.
Meestal verdraagt de patiënt deze therapie goed. Soms treedt enkele dagen na therapie het “postembolisatiesyndroom” op: vermoeidheid, koorts, abdominale last en nausea. Behandeling daarvan kan met klassieke analgetica en anti-emetica.
Zeldzame ernstige bijwerkingen (tot 90 dagen na therapie) zijn meestal het gevolg van radiatieschade door ongewilde extrahepatische depositie van 90Y-sferen of van overdosering (radiation-induced liver disease). Een juiste patiëntenselectie en het nauwgezet uitvoeren van de procedure vermindert het risico op deze ernstige complicaties sterk. Er zijn standaard vier partijen bij de samenwerking betrokken: de hepatoloog, de oncoloog, de interventioneel radioloog en de nuclearist.
In de praktijk wordt TARE toegepast bij inoperabel hepatocellulair carcinoma als palliatieve therapie of in afwachting van een curatieve levertransplantatie. Bij levergemetastaseerde colorectale of neuro-endocriene tumoren waarvoor geen (chemo)therapeutische opties meer voorhanden zijn, kan TARE de tumorprogressie afremmen. Studies zijn lopende om na te gaan of TARE toegediend in een vroeger stadium een overlevingsvoordeel kan bieden.
Referenties
1. Radioembolisatie voor de behandeling van leverkanker: een praktische handleiding. Dr. M.G.E.H. Lam, Drs. J.E. Huijbregts, Prof. dr. M.A.A.J. van den Bosch, Dr. F.D. van het Schip, Dr. J.F. Nijsen, Dr. B.A. Zonnenberg. Tijdschrift voor Nucleaire Geneeskunde, jaargang 34, 2012, nummer 2.
2. Hepatocellular carcinoma: ESMO-ESDO Clinical Practice guidelines for diagnosis, treatment and follow-up, Annals of Oncology 23 (Supplement 7): vii41-vii48, 2012.
3. Neuroendocrine bronchial and thymic tumors: ESMO Clinical Practice guidelines for diagnosis, treatment and follow-up, Annals of Oncology 23 (Supplement 7): vii120-vii123, 2012.
4. Metastatic colorectal cancer: ESMO Clinical Practice guidelines for diagnosis, treatment and follow-up, Annals of Oncology 25 (Supplement 3): iii1-iii9, 2014.
Download het artikel als PDF-bestand
Copyright © 2015 AZ Sint-Jan Brugge-Oostende AV. Alle rechten voorbehouden. De inhoud (zowel teksten als afbeeldingen) van dit magazine is auteursrechtelijk beschermd. Niets uit deze uitgave mag vermenigvuldigd of doorgegeven worden aan derden zonder schriftelijke toelating van de uitgever.