Een 35-jarige man komt op consultatie met ademhalingsgebonden pijn in het rechterhypochondrium. De pijn is er sinds een tweetal weken en straalt uit naar de rechterschouder. Bij navraag vermeldt de patiënt een gewichtsverlies van 17 kg op vier maanden tijd, hoewel hij zijn eetlust bewaarde, en ook nachtzweten zonder duidelijke koorts.
In de voorgeschiedenis wordt de aandacht getrokken door frequente hospitalisaties wegens infectie tot de leeftijd van twee jaar en een episode van niet verder gedifferentieerd reumatologisch lijden op tienjarige leeftijd. De patiënt ondernam geen tropische reizen en heeft een kat die net geen jaar oud is. Klinisch onderzoek brengt weinig bijzonderheden aan het licht. De patiënt is koortsvrij. Het lichaamsgewicht bij opname is 61 kg, de bloeddruk is 134/71 mmHg en de polsfrequentie 89/min. Biochemisch onderzoek wijst op een licht inflammatoir bloedbeeld (leukocytose: 11000/μL met 76% neutrofielen, C-reactieve proteïne: 38 mg/L) met een stabiele nierfunctie en een normaal ionogram, alsook licht verstoorde leverparameters (alkalische fosfatasen: 191 U/L, GGT: 63 U/L).
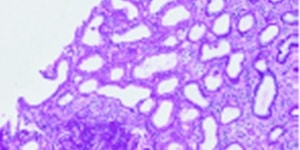
Figuur 1: Histopathologisch beeld van granulomateus infiltraat met centrale necrose
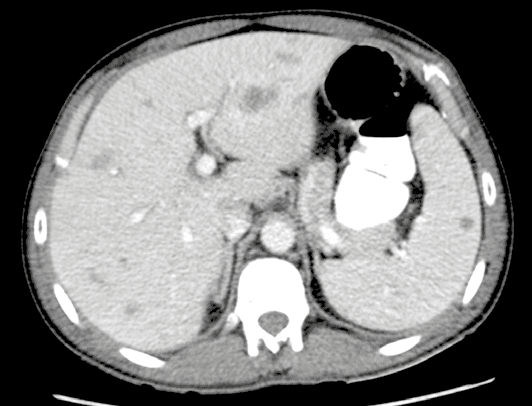
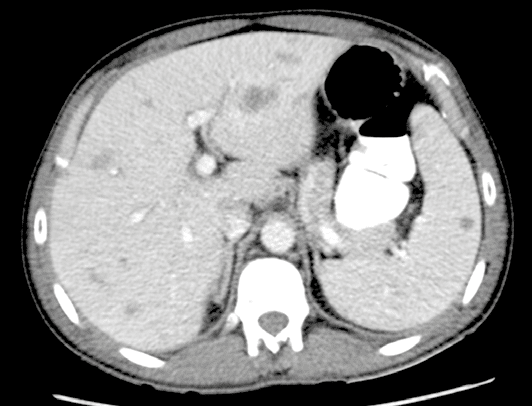
Het urinesediment, de auto-immuunserologie en de respiratoire infectieuze screening blijken negatief. Een CT-scan van het abdomen toont capterende lever- en miltletsels met aanliggend oedeem en verspreide intra-abdominale adenopathieën; een CT-scan van de thorax duidt op adenopathieën ter hoogte van de axillae, de halsbasis en in het mediastinum. Een echogeleide punctie van een subcapsulair gelegen leverletsel toont bij anatomopathologisch onderzoek necrotiserende granulomen en een opvallende veneuze stuwing, en bij microbiologisch onderzoek witte bloedcellen met gramnegatieve bacillen in de gramkleuring, maar met een steriele kweek.
De man vertoont dus een systemisch inflammatoir proces met gedissemineerde granulomateuze letsels in de lever, miltletsels en adenopathieën boven en onder het diafragma.
Oplossing
Het klinisch beeld doet in eerste instantie denken aan een infectieuze pathologie die zich presenteert met necrotiserende granulomen. Er volgt een een ‘total body’ PET-CT-scan en een uitgebreid serologisch onderzoek naar Treponema pallidum, Bartonella spp., Brucella spp., Coxiella burnetii, Toxoplasma gondii, Strongyloides, Echinococcus, HIV, TBC en moleculaire SOA-testen. Dunnedarmbiopten sluiten de ziekte van Whipple uit.
Figuur 2: CT-beeld van granulomateuze letsels in lever en milt
Een indirecte immuunfluorescentietest bevestigt een sterk positieve Bartonella-serologie, indicatief voor een actieve infectie, met een B. henselae IgG-titer van 1/16.000 en een B. quintana IgG-titer van 1/8.000. De diagnose is een hepatosplenische vorm van de kattenkrabziekte.
De kattenkrabziekte wordt veroorzaakt door B. henselae, een traag groeiende gramnegatieve bacil. Het genus Bartonella kent ten minste drie species die pathogeen zijn voor de mens (zie tabel 1).
|
Tabel 1: Epidemiologie van humane pathogene Bartonella species |
|||||
| Species | Klinische manifestatie (immuuncompetent) | Klinische manifestatie (gecompromitteerd) | Reservoir | Vector/ transmissie | Geografische verspreiding |
| B. henselae | Kattenkrabziekte, atypische presentaties, endocarditis | Bacillaire angiomatosis, peliosis van lever en milt, bacteriëmisch syndroom met koorts, endocarditis | Kat (vooral jonge) | Via krabletsel (of beet) van kat, mogelijk via kattenvlo | Wereldwijd |
| B. quintana | Loopgravenkoorts, bacteriëmisch syndroom met koorts, endocarditis, asymptomatische drager | Idem als B. henselae | Mens | Luis | Wereldwijd, onder slechte hygiënische omstandigheden |
| B. bacilliformis | Oroya-koorts en verruga peruana (ziekte van Carrión), asymptomatische drager | Onbekend | Mens | Zandvlieg | Peru, Ecuador |
| Atypische presentatie: vnl. infecties van lever, milt, oog, centraal zenuwstelsel, hart en botten | |||||
De B. henselae-infectie wordt op de mens overgedragen via een beet of krabletsel van een besmette kat of, in mindere mate, via een vlooienbeet. Bij 90% van de patiënten komt de ziekte tot uiting als een gelokaliseerde, prominente lymfadenitis. Deze treedt gewoonlijk twee weken na inoculatie op en gaat meestal gepaard met milde, veralgemeende klachten van algemene malaise, anorexie, lichte koorts en abdominale last. Circa 10% van de patiënten vertoont een gedissemineerde, ernstigere vorm, waarbij de bacterie zich verspreidt naar andere orgaansystemen (zie tabel 2). De geschatte incidentie in België bedraagt 2 op 100.000 inwoners[4], maar vermoedelijk is dit een forse onderschatting van de reële incidentie, in het licht van de Nederlandse cijfers: 12,5 op 100.000 inwoners. Bartonellose komt voornamelijk voor bij jonge, immuuncompetente patiënten, waarbij de bacterie slechts zelden een ernstige pathologie veroorzaakt.
|
Tabel 2: Atypische presentatie van kattenkrabziekte |
|
| Orgaan | Symptomatologie |
| Huid | Lokale huidafwijkingen ter plaatse van het krabletsel, beet (vaak), erythema multiforme, erythema nodosum, trombocytopenische purpura |
| Lymfeklieren | Langdurige lymfeklierzwelling (vaak), 10% abcedering |
| Inwendige organen | Granulomateuze laesies in lever en/of milt, glomerulonefritis |
| Zenuwstelsel | Encefalopathie, convulsies, coma, myelitis, perifere neuropathie |
| Oog | Conjunctivitis van Parinaud, neuroretinitis, uveïtis, iridocyclitis, glaucoom |
| Bloed | Hemolytische anemie, trombocytopenische purpura |
| Bot/gewrichten | Artritis, osteomyelitis |
| Hart | Endocarditis, myocarditis |
De diagnose berust op de vrij typische klinische presentatie samen met een anamnese van kattencontact, hoewel de patiënt zich in meer dan de helft van de gevallen geen kattencontact herinnert. Ze wordt bevestigd door een serologische test en/of polymerasekettingreactietest op klierweefsel of punctievocht. Bij volwassenen is het steeds nodig om de Bartonella IgG naast de IgM te bepalen. IgG-titers van 1/320 of 1/1.000 zonder aanwezigheid van IgM duiden voornamelijk op oude infecties, terwijl IgG-titers > 1/1.000, met of zonder aanwezigheid van IgM, vaak geassocieerd zijn met recente en nog actieve infecties – zoals in deze casus.
Indien men te maken krijgt met een ‘atypisch’ klachtenpatroon, met aanwezigheid van adenopathieën en een vermoeden van granulomateuze infectie, dan is het aangewezen om kattenkrabziekte te overwegen in de differentiaaldiagnose (zie tabel 3). In geval van een ongecompliceerde infectie hebben immuuncompetente patiënten geen antibacteriële therapie nodig. Hun symptomen verdwijnen spontaan na enkele weken. In deze casus kreeg de patiënt, gezien de geassocieerde hepatosplenische aantasting, gedurende zes weken een behandeling met doxycycline 100 mg (2x/dag) samen met rifampicine 600 mg (1x/dag).
|
Tabel 3: Differentiaaldiagnose van granulomen in de lever |
|
| Infectieus | |
| Bacterieel | Tuberculose (M. tuberculosis, M. bovis), lepra (M. leprae), brucellose (B. abortus), syfilis (T. pallidum) – zelden: tularemie (F. tularensis), listeriose (L. monocytogenes), kattenkrabziekte (B. henselae), Q-koorts (C. burnetii) |
| Parasitair | Toxoplasmose (T. gondii), Schistosomiasis, viscerale larva migrans (Toxocara spp.), fasciolose (F. hepatica), ascariasis (Ascaris spp.) |
| Fungaal | Histoplasmose, coccidioïdomycose, candidiasis, aspergillose, nocardiose, cryptococcose |
| Viraal | Cytomegalovirus, epstein–barrvirus, HIV, hepatitisvirussen |
| Niet infectieus | |
| Sarcoïdose | |
| Chronische inflammatoire darmziekten | |
| Primaire biliaire cirrose | |
| Maligniteit | Ziekte van Hodgkin, non-Hodgkinlymfoom |
| Metaalintoxicatie | |
| Vasculitis | Lupus erythematodes disseminatus |
| Polyarteriitis nodosa | |
| Reumatoïde artritis | |
| Ziekte van Wegener | |
| Reactie op medicatie | |
| Reactie op corpora aliena | |
Voor meer informatie:
apr. Steven De Keukeleire
assistent klinisch bioloog in opleiding
dr. Marijke Reynders
dienst Laboratoriumgeneeskunde
dr. Stefaan Vandecasteele
dienst Inwendige Ziekten
Download het artikel als PDF-bestand.
Copyright © 2015 AZ Sint-Jan Brugge-Oostende AV. Alle rechten voorbehouden. De inhoud (zowel teksten als afbeeldingen) van dit magazine is auteursrechtelijk beschermd. Niets uit deze uitgave mag vermenigvuldigd of doorgegeven worden aan derden zonder schriftelijke toelating van de uitgever.