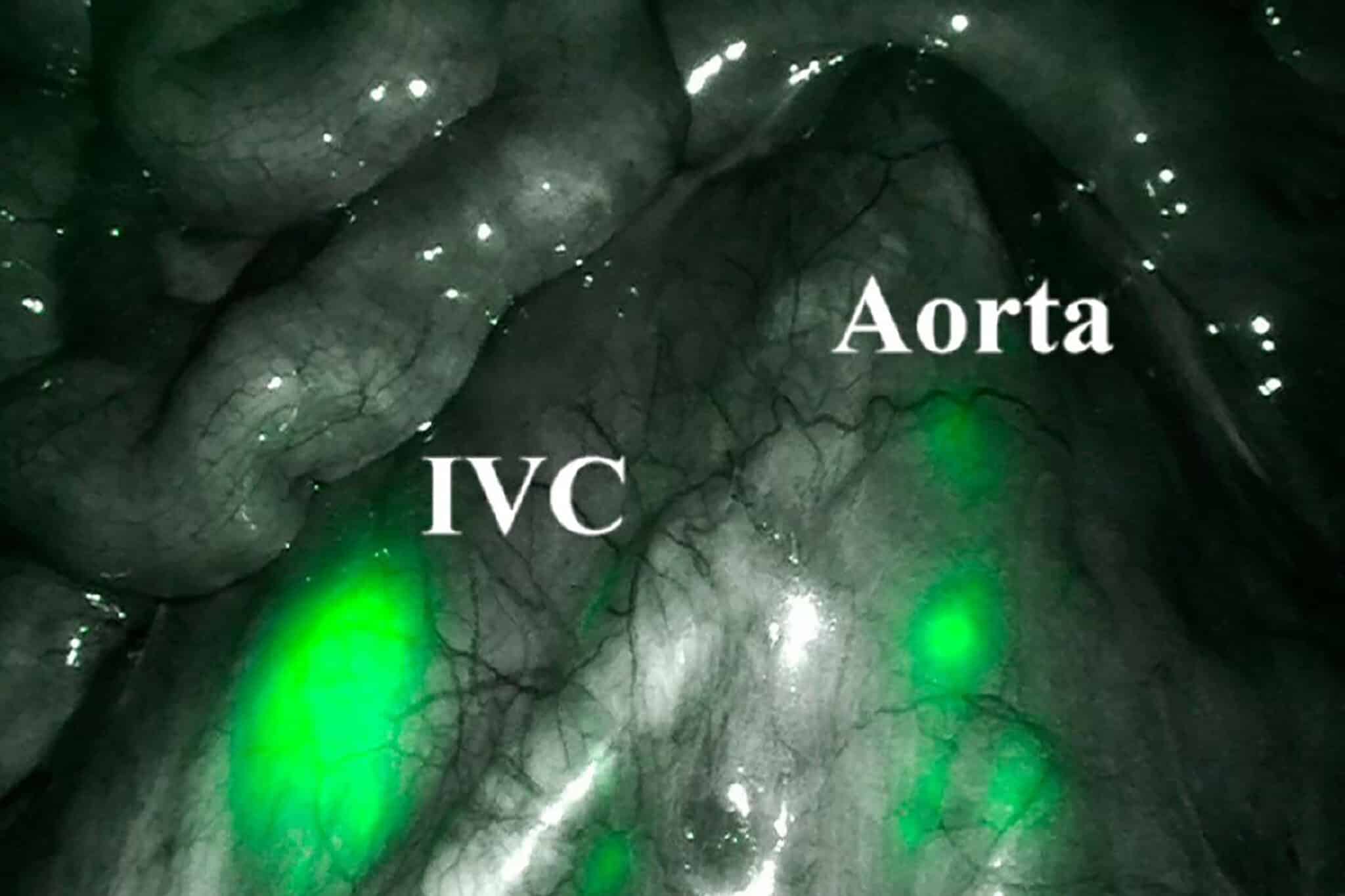
Brachytherapie is een inwendige bestraling waarbij gesloten radioactieve bronnen (bv. cesium-137, iridium-192 of jodium-125) in of tegen het te bestralen weefsel worden gebracht. Aangezien de stralingsdosis beperkt blijft tot de zone rond de bron, maakt brachytherapie het mogelijk om de omliggende gezonde weefsels optimaal te sparen, met minder nevenwerkingen als gevolg.
Toepassing
Doorheen de jaren zijn verschillende technieken heel wat geoptimaliseerd op het vlak van effectiviteit en veiligheid, waardoor brachytherapie vandaag een belangrijke rol speelt in de bestralingsbehandeling van bepaalde vastweefseltumoren. Artsen passen brachytherapie toe als enige behandeling of als aanvullende behandeling na een uitwendige bestraling. Afhankelijk van de indicatie bestaan er uiteenlopende technieken: o.a. brachytherapie met radioactieve zaadjes voor prostaatkanker, contact-brachytherapie voor bepaalde types van huidkanker en brachytherapie van de baarmoeder(hals) via intravaginale of uterovaginale applicatoren.
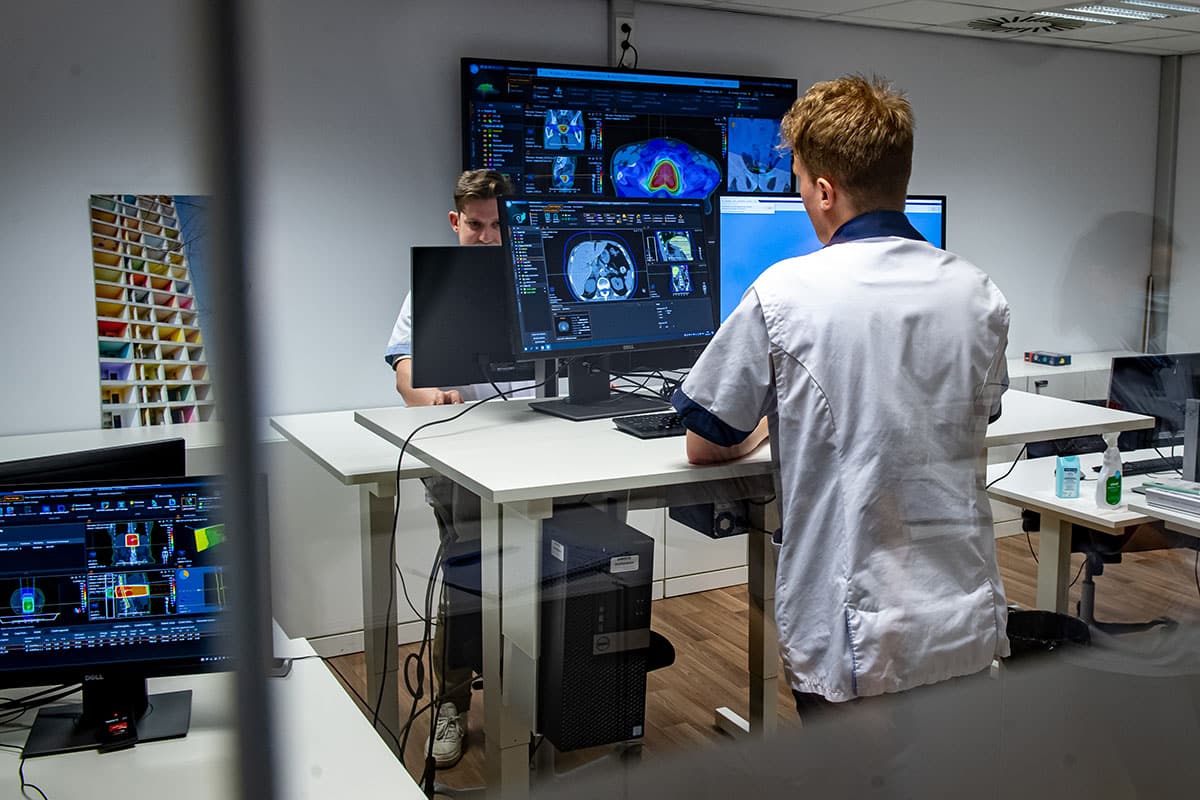
Na optimalisatie van de dosisverdeling worden de applicatoren aangesloten op een bestralingsmachine.
Recent installeerde de dienst Radiotherapie van het Oncologisch Centrum in het AZ Sint-Jan Brugge-Oostende AV een HDR of “High-Dose Rate” brachytherapietoestel, aangewend in de bestralingsbehandeling van patiënten met een cervix- of endometriumcarcinoom, alsook ter behandeling van kleine (niet-melanoma) huidtumoren. Het Oncologisch Centrum is in deze setting het enige in West-Vlaanderen dat deze bestralingsvorm aanbiedt.
Brachytherapie in de gynaecologische oncologie
Patiënten met een baarmoederhals-, baarmoeder-, vagina- of vulvacarcinoom kunnen tijdens hun behandeling in aanmerking komen voor brachytherapie, meestal als bijkomende “boostbestraling” in combinatie met een externe bestralingsreeks – al dan niet na een heelkundige ingreep. Gezien deze tumoren vrij toegankelijk zijn via vaginale weg, laat brachytherapie toe om een uitstekende lokale tumorcontrole te bereiken zonder de gezonde weefsels in de buurt te belasten, en dit zelfs bij lokaal uitgebreide tumorstadia van baarmoederhalskanker. Indien brachytherapie ongeschikt is na een externe bestraling, bijvoorbeeld omdat het tumorvolume te groot is, dan wordt de boostdosis gegeven met behulp van externe radiotherapie.
Het Oncologisch Centrum van het AZ Sint-Jan Brugge-Oostende AV maakt momenteel gebruik van een “High-Dose Rate” techniek, waarbij de arts via een iridium-192-bron een hoge dosis toedient in een korte tijdspanne. Voordien werd een “Low-Dose Rate” techniek gebruikt, waarbij de bestraling (met een cesium-137-bron) zich over een langere periode voltrok. Gelijktijdig met de implementatie van de HDR-techniek schakelde het centrum over van een 2D-beeld- naar een 3D-beeldgebaseerde brachytherapieplanning, conform de Europese richtlijnen.[1] Dit zorgt voor een uitermate nauwkeurige dosisberekening, zowel ter hoogte van het doelgebied als de omliggende gezonde organen.
Methode

Eerste type applicator: uterieme tandem met colpostaten.
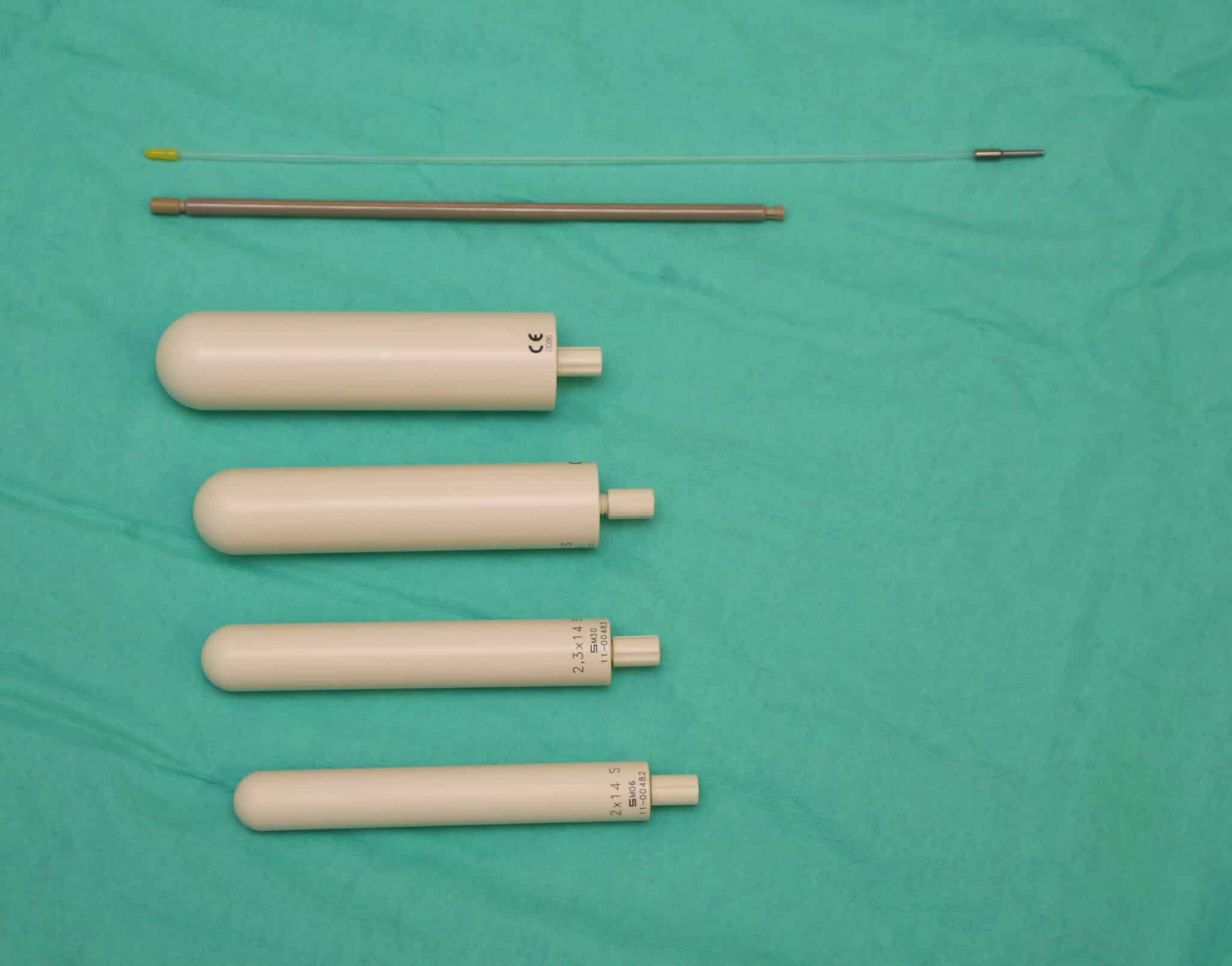
Tweede type applicator: vaginale cilinder.
Er bestaan verschillende types applicatoren (holle buisjes voor het inbrengen van radioactieve bronnen) die via de vagina tot tegen of in de vaginakoepel of baarmoeder(hals) geplaatst kunnen worden.
Met de ingebrachte applicator ter plaatse neemt de arts een CT- en/of MRI-scan om zo een nauwkeurige dosisverdeling te berekenen, met als doel een optimale bestraling te garanderen. Na optimalisatie van de dosisverdeling worden de applicatoren aangesloten op een bestralingsmachine van waaruit de radioactieve bron – in dit geval iridium-192 – in de holle buisjes geschoven wordt. Dit zogenaamde “after-loading” systeem maakt het mogelijk om het toestel te bedienen van buiten de kamer, zodat de verpleegkundige en arts zelf niet met de bestralingsbronnen in contact komen.

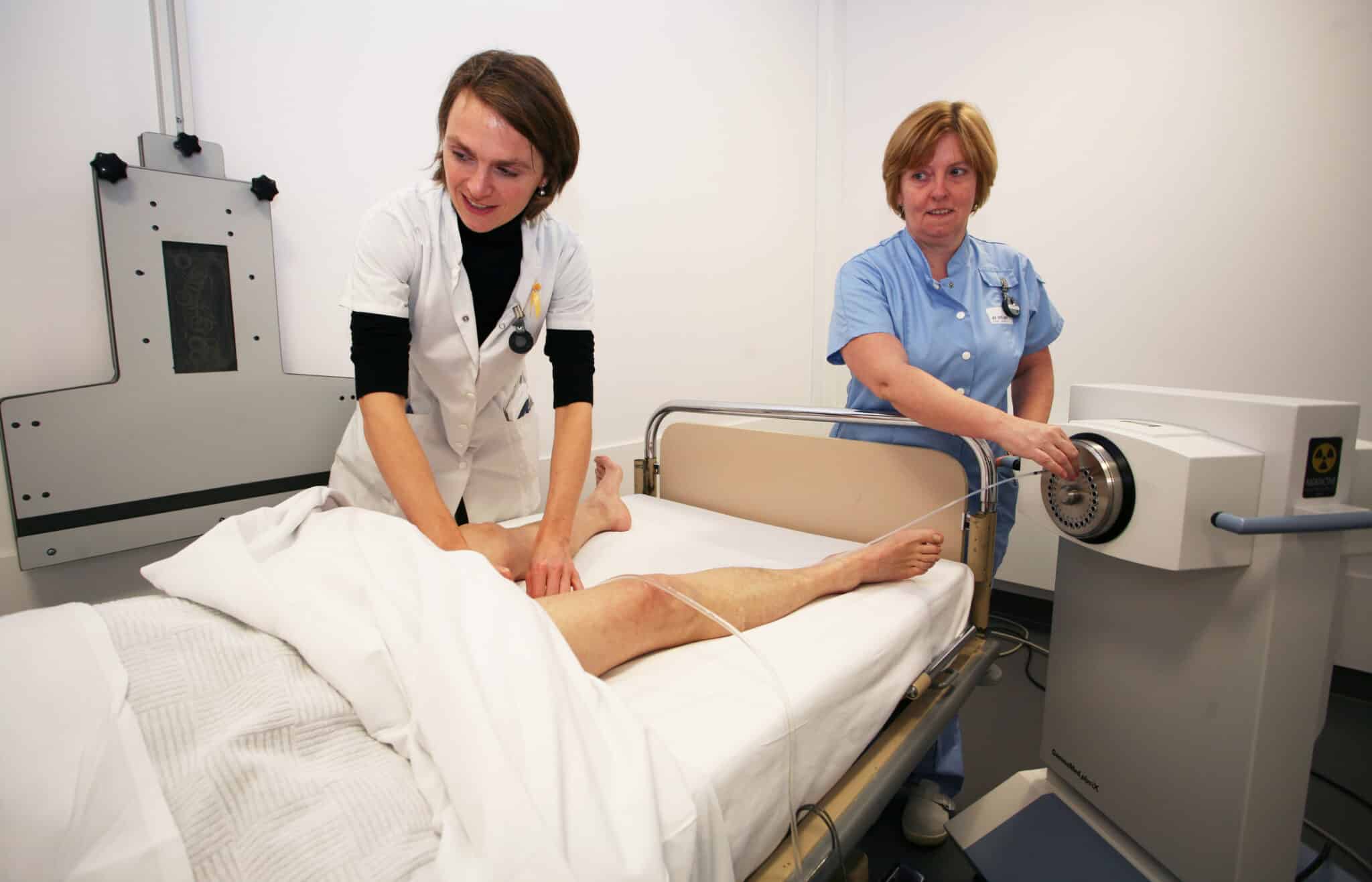
De “after-loader” vermijdt rechtstreeks contact tussen de zorgverleners en de bestralingsbron.
Patiënten worden per sessie ongeveer een halve dag opgenomen. Per week vinden één à twee sessies plaats; in totaal ondergaat de patiënt drie tot vier sessies. Mogelijke risico’s tijdens zo’n inwendige bestraling situeren zich zowel op het niveau van stralingsbescherming als op klinisch vlak. Er bestaat bijvoorbeeld een risico op perforatie tijdens de applicatie, alsook een beperkt risico op cystitis en/of rectitis na elke fractie. Elke behandeling vergt dan ook een nauwkeurige voorbereiding, een vlotte samenwerking tussen artsen, verpleegkundigen en stralingsfysici, alsook strikte regels van stralingsbescherming.
Bij elke applicatie, die in de regel steriel gebeurt, verifieert de arts op een CT- of MRI-scan de positie van de applicator tegenover het doelvolume en sluit hij een mogelijke perforatie uit. Pas dan kan het bestralingsplan opgemaakt worden. Hierbij evalueren de arts en de fysicus de dosisverdeling op doelvolume en omliggende organen, rekening houdend met de voorgeschreven richtlijnen en tolerantielimieten.
Voor de start van de behandeling kijkt men de aansluiting na van de applicatoren aan de after-loader. De bronposities en de toegankelijkheid van de catheters worden automatisch getest. De behandeling gebeurt in een met lood en barietbeton afgeschermde kamer, voorzien van de nodige stralingsbeschermingsmaatregelen. Een camera garandeert continue visuele controle van de patiënt.
Resultaten
Sinds de invoering van de HDR-techniek en de 3D-beeldgebaseerde planning in mei 2013 werden reeds 17 patiënten succesvol behandeld:
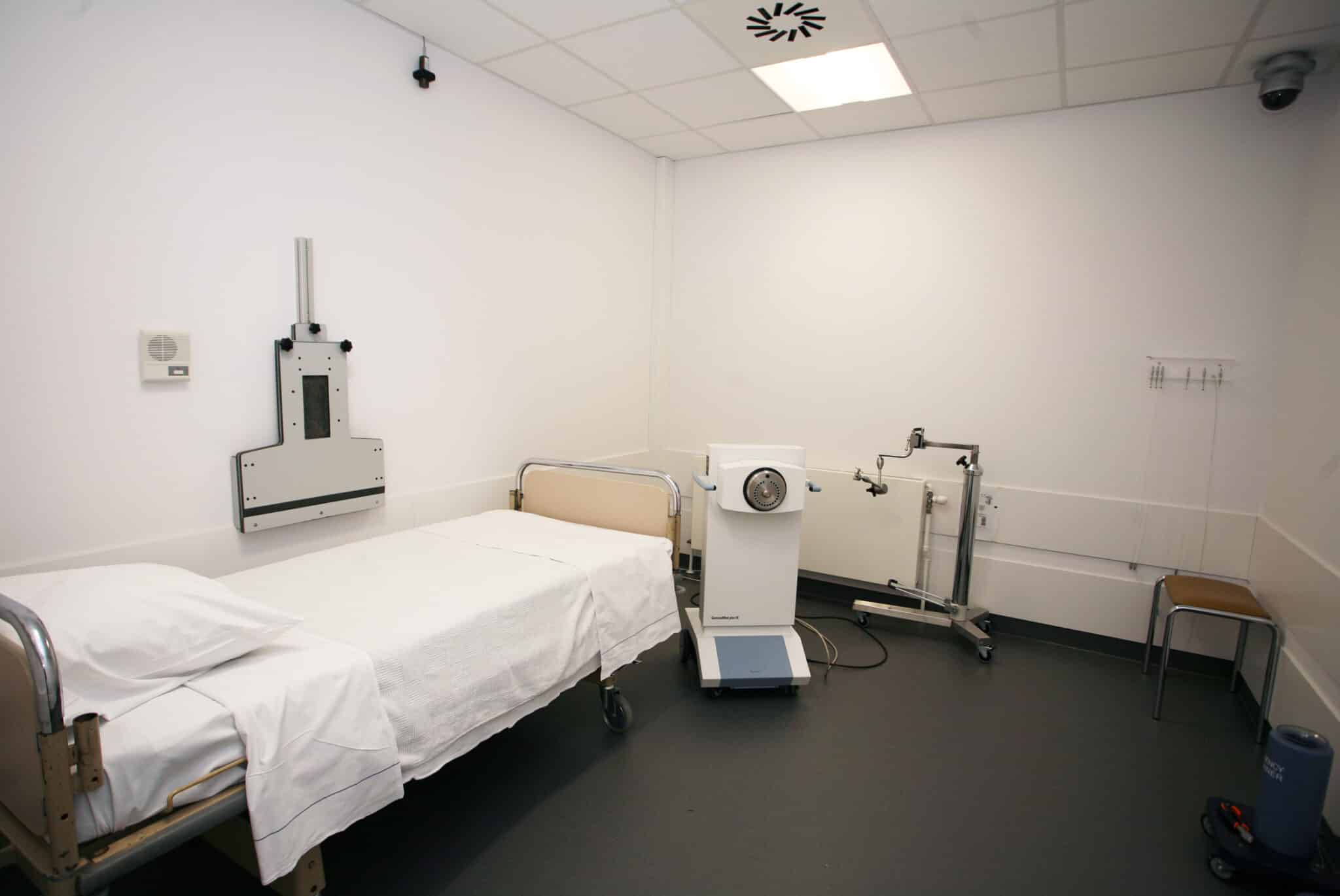
De behandeling gebeurt in een met lood en barietbeton afgeschermde kamer, voorzien van de nodige stralingsbeschermingsmaatregelen en een camera.
- 4 patiënten ondergingen uterovaginale brachytherapie als aanvullende boostbestraling op de tumor in de baarmoederhals, na externe pelvisbestraling.
- 13 patiënten kregen vaginale brachytherapie – al dan niet na externe pelvisbestraling – postoperatief, waarvan 8 patiënten voor een endometriumcarcinoom en 3 patiënten voor een cervixcarcinoom.
- 2 patiënten ondergingen vaginale brachytherapie na externe pelvisbestraling voor een recidief endometrium/cervixcarcinoom.
De tolerantie bij deze patiënten was vrij hoog; enkele patiënten vermeldden lokaal ongemak tijdens de applicatie van de uteriene tandem. Eenmalig kon de behandeling niet doorgaan, nadat beeldvorming wees op een progressie van de tumor in de vagina. Brachytherapie is dan geen valabele optie meer.
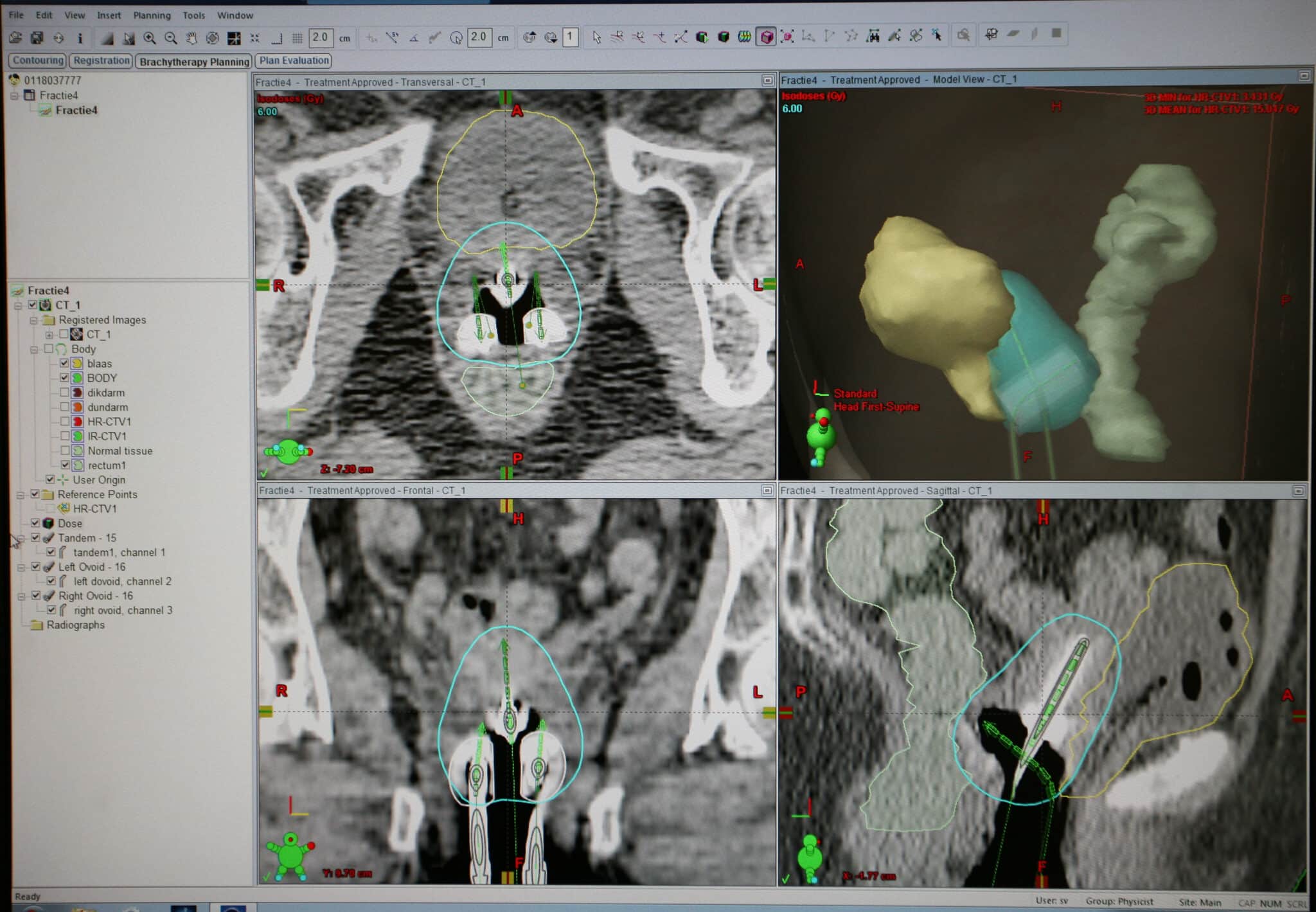
Deze 3D-beeldgebaseerde brachytherapieplanning onderscheidt de regio met hoge dosis (blauw) ten opzichte van de omliggende organen.
Bij een andere patiënte werd de positionering afgekeurd op de CT-scan, vermoedelijk te wijten aan een verplaatsing van de applicatoren tijdens transport, ondanks fixatie aan de bekkenbodem. De volgende behandelingen bij deze patiënte verliepen probleemloos.
Na elke behandeling is er op korte termijn een beperkte kans op bloeding of infectie. Één patiënte ontwikkelde een blaasinfectie tussen twee fracties in en kreeg een klassieke behandeling met antibiotica. Op langere termijn kan het slijmvlies van de vagina minder elastisch en droger worden. In dat geval versmalt de vagina en kunnen er vergroeiingen ontstaan. Elke patiënte krijgt hiervoor een vaginale gel voorgeschreven.
Conclusie
Het invoeren van de HDR-brachytherapietechniek en de 3D-beeldgebaseerde dosisplanning zorgt voor een optimalisatie van de bestralingsbehandeling, wat op zijn beurt resulteert in een betere tumorcontrole en hogere zorgkwaliteit binnen de gynaecologische oncologie.
Referentie
- Recommendations from gynaecological (GYN) GEC ESTRO working group (II): concepts and terms in 3D image-based treatment planning in cervix cancer brachytherapy-3D dose volume parameters and aspects of 3D image-based anatomy, radiation physics, radiobiology. Pötter R, Haie-Meder C, Van Limbergen E, Barillot I, De Brabandere M, Dimopoulos J, Dumas I, Erickson B, Lang S, Nulens A, Petrow P, Rownd J, Kirisits C; GEC. ESTRO Working Group. Radiother Oncol. 2006 Jan;78(1):67-77. Epub 2006 Jan 5.